光合作用是地球上最重要的化学反应,1988年诺贝尔化学奖颁发给了紫色光合细菌光反应中心的晶体结构1。这是世界上第一个膜蛋白晶体结构,颠覆了人们对膜蛋白结晶学的认识,也开辟了光合膜蛋白结构与功能研究的新时代。然而三十年来,人们对紫细菌光合反应中心与外围天线蛋白复合体联系仍不清楚,其与外界的物质和能量交换机制也无结构生物学证据支持。
本期(2018年4月5日)在线发表的两篇Nature长文分别报道了高分辨率的反应中心和天线的超级复合体结构(LH1-RC)2,3。这是继2014年日本茨城大学王征宇团队与合作者解析了紫色光合细菌Thermochromatiumtepidum晶体结构(Niwa et al 2014)之后4,此研究领域迎来的终极突破。日本冈山大学沈建仁团队与王征宇团队合作再次将Tch.Tepidum的LH1-RC晶体分辨率提高到1.9埃。此高分辨率晶体结构揭示了LH1-RC蛋白和多种辅因子更加清晰的精细结构,与1988年诺奖的反应中心结构相比,此超级复合体结构描绘了反应中心结合外围天线的状态,描述了中心与天线(16组α和β亚基对)的结合方式(图1),以及天线复合体中钙离子的准确位置和结合环境。也对醌转移单子的路径和机制进行了描述。

同时,英国谢菲尔德大学的Hunter教授团队通过冷冻电镜技术对Blastochloris viridis的LH1-RC复合体进行了结构解析,分辨率为2.9埃。此紫色光合细菌即是当年获诺贝尔奖的菌株,Tch.tepidum为其“兄弟”。相比于Tch.Tepidum,Bch. viridis的LH1-RC复合体外围共17对α和β亚基,而且多了一圈γ亚基(16个)。缺失的一个γ亚基刚好作为醌转移单子的通道,而且在复合体内部完美地发现了Qp的口袋位点(图2)。这两个long-awaited高分辨率LH1-RC结构,在时隔三十年以后,为掀起膜蛋白结构生物学研究热潮的光合紫细菌反应中心的结构研究画上了完美句号。
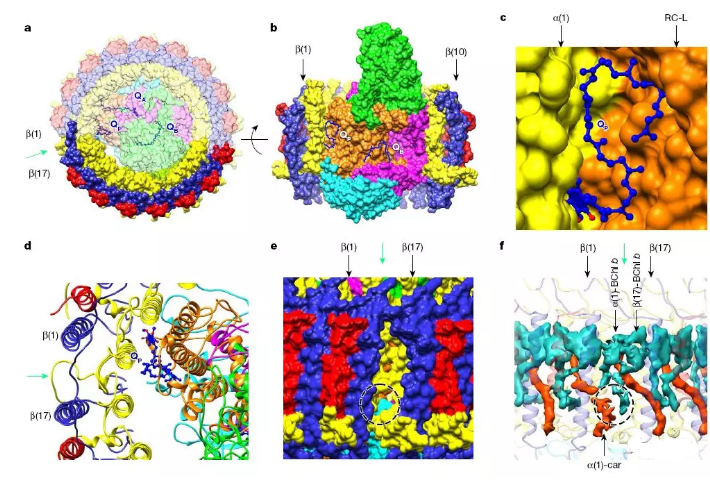
虽然国内在高等植物和红藻的光合蛋白结构解析方面领先世界,但关于光合细菌的研究工作还开展较少。而很多光合细菌是出自火山和热泉众多的岛国日本,风行于欧美,但参与这两项主要工作的第一作者都是国人,钱朴博士致力于此项研究已逾二十载,于龙江博士也是2014年晶体结构的主要完成人之一。沈建仁教授和王征宇教授更是在光合作用研究领域的国际知名专家,更是华人科学界的骄傲!
Refer:
1 Deisenhofer,J., Epp, O., Miki, K., Huber, R. & Michel, H. Structure Of the ProteinSubunits In the Photosynthetic Reaction Center Of Rhodopseudomonas-Viridis at3a Resolution. Nature 318, 618-624 (1985).
2 Yu, L.-J.,Suga, M., Wang-Otomo, Z.-Y. & Shen, J.-R. Structure of photosyntheticLH1–RC supercomplex at 1.9 Å resolution. Nature, doi:10.1038/s41586-018-0002-9(2018).
3 Qian, P.,Siebert, C. A., Wang, P., Canniffe, D. P. & Hunter, C. N. Cryo-EM structureof the Blastochloris viridis LH1–RC complex at 2.9 Å. Nature,doi:10.1038/s41586-018-0014-5 (2018).
4 Niwa, S. etal. Structure of the LH1-RC complex from Thermochromatium tepidum at 3.0 A.Nature 508, 228-232, doi:10.1038/nature13197 (2014).