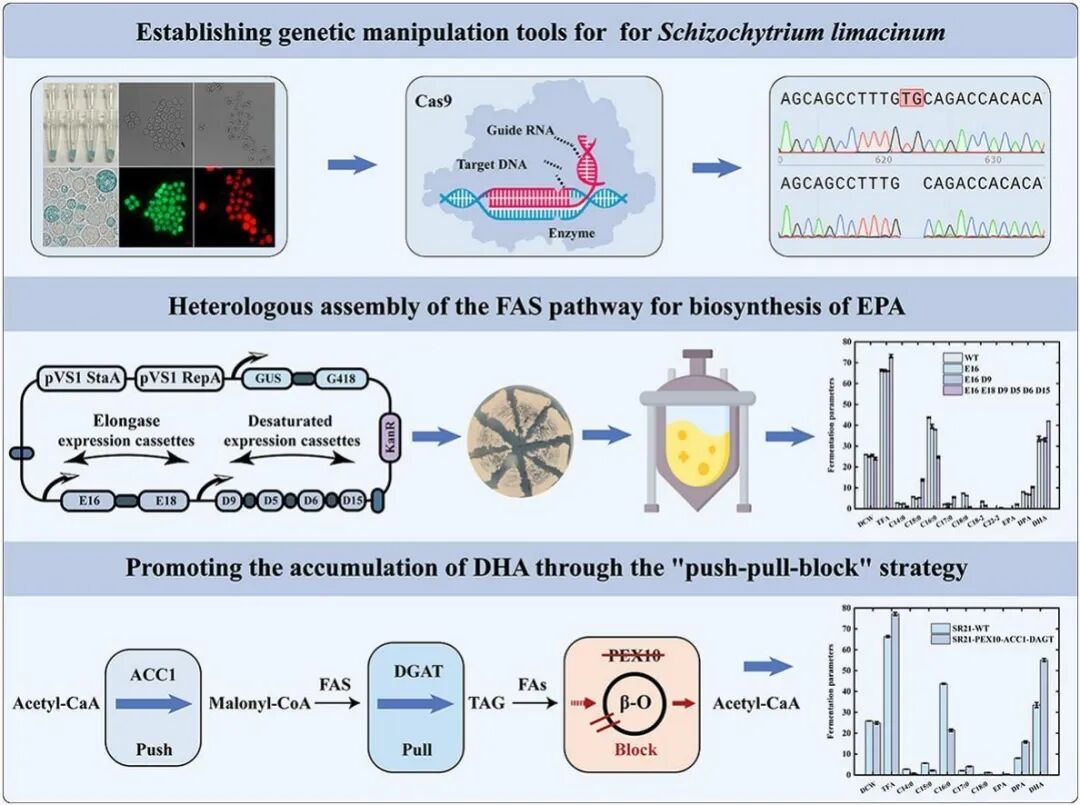
CRISPR/Cas系统凭借其高灵活性与高效性,已在多种产油微生物的遗传改造中获得成功应用,为微生物代谢工程领域提供了强大技术支撑。然而,裂殖壶菌(Schizochytrium limacinum)作为一种极具潜力的多不饱和脂肪酸(PUFA)生产菌株,其尚不完善的遗传转化体系严重限制了该菌株的进一步开发与广泛应用,成为制约其代谢工程改造的关键瓶颈。
为突破这一技术局限,本研究针对性地构建了一种新型农杆菌介导筛选系统,创新采用基于乙酸盐的筛选策略,有效提升了裂殖壶菌SR21的遗传转化效率,相较于原始转化体系,转化效率显著提升77.13%,为后续基因编辑及代谢工程改造奠定了坚实基础。与此同时,研究开发了一种由裂殖壶菌内源Pol III启动子(tRNAGly)驱动的CRISPR/Cas9表达系统,成功在裂殖壶菌SR21中实现高效基因编辑,编辑效率达到48.38%,解决了该菌株基因编辑效率低下的核心问题。
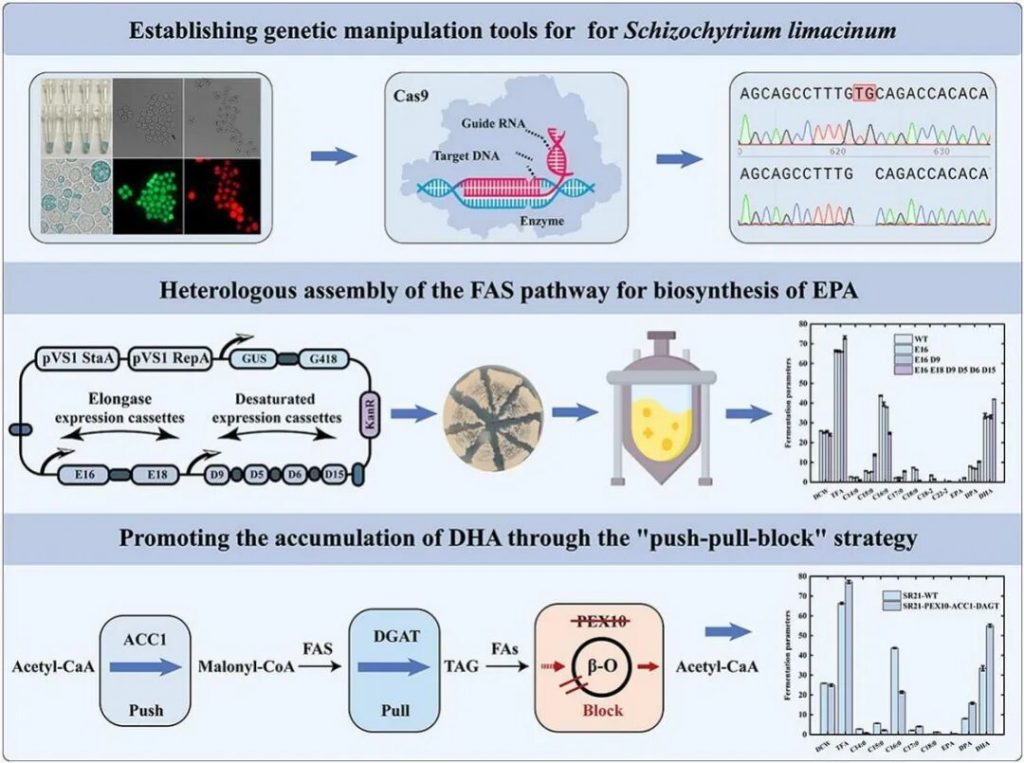
在建立高效遗传转化与基因编辑体系的基础上,研究进一步对裂殖壶菌SR21进行代谢工程改造,核心目标为高效生产DHA(二十二碳六烯酸)和EPA(二十碳五烯酸)两种重要多不饱和脂肪酸。针对EPA的合成需求,研究对裂殖壶菌SR21中不完整的脂肪酸合酶(FAS)途径进行代谢重组,成功实现了源自FAS途径的EPA从头合成,填补了该菌株通过FAS途径合成EPA的技术空白。
对于DHA的高效合成,研究实施“推-拉-阻(push-pull-block)”代谢工程策略,重点强化裂殖壶菌SR21中固有的聚酮合酶(PKS)途径,通过调控代谢流分布,推动碳源向DHA合成方向高效分配。实验结果显示,与野生型裂殖壶菌SR21相比,改造后的工程菌株油脂含量显著提升至77.14%,其中DHA含量提升至55.10%,多不饱和脂肪酸(PUFA)总含量提升至70.47%,实现了目标产物产量的大幅提升。
综上,本研究的核心贡献主要体现在三个方面:一是构建的新型农杆菌介导筛选系统,显著提升了裂殖壶菌的转化效率,为该菌株的遗传转化研究提供了宝贵的技术参考;二是开发的内源启动子驱动CRISPR/Cas9系统,为推进裂殖壶菌SR21的代谢工程改造提供了稳定可靠的技术支撑;三是获得的基因工程菌株SR21-ΔPEX10-ACC1-DGAT,具备通过进一步发酵优化生产高纯度DHA的巨大潜力。此外,本研究实现的FAS途径异源组装,为未来通过PKS与FAS双途径联产多不饱和脂肪酸提供了一种新颖且可行的技术策略,对推动微生物法生产PUFA的工业化发展具有重要意义。
原文链接: CRISPR/Cas9-mediated metabolic engineering for enhanced PUFA production in Schizochytrium limacinum