为实现高附加值倍半萜类化合物(+)-诺卡酮的绿色高效合成,解决传统化学合成步骤繁琐、环境污染严重及植物提取产量低下等问题,本研究以莱茵衣藻为模式宿主,系统开展了(+)-诺卡酮合成关键酶——瓦伦烯合酶与瓦伦烯氧化酶的体内功能表征,为代谢途径的构建奠定了坚实基础。研究通过体外酶活检测与体内异源表达验证,明确了两种关键酶的催化活性、底物特异性及表达规律,排除了酶活不足、底物竞争等潜在瓶颈,成功构建出从上游前体到目标产物(+)-诺卡酮的完整异源代谢途径,实现了目标产物的初步合成。
针对微藻体内MEP(2-甲基-D-赤藓糖醇-4-磷酸)途径碳通量不足、前体物质法尼基焦磷酸(FPP)供应有限的问题,本研究采用融合酶设计策略对MEP途径进行精准优化。通过将MEP途径关键酶与瓦伦烯合酶进行合理融合,缩短了酶与底物之间的空间距离,减少了中间产物的扩散损失,有效提高了碳通量向目标产物合成方向的分配效率。同时,充分利用莱茵衣藻叶绿体中丰富的FPP资源库,规避了胞质中FPP向其他代谢支路的分流,进一步强化了异源倍半萜合成的前体供应,显著提升了(+)-诺卡酮的合成效率。
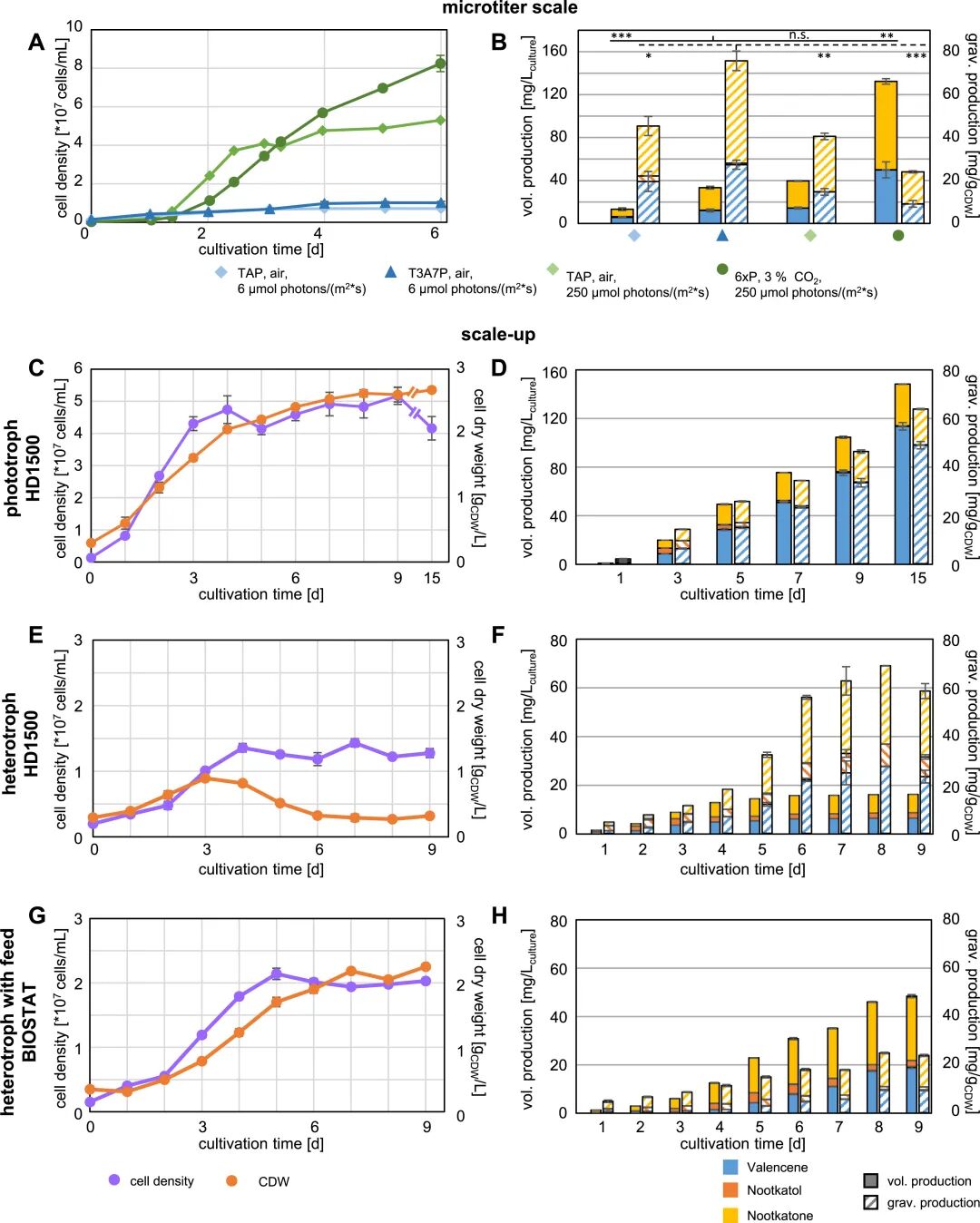
光和碳源作为微藻生长与代谢合成的核心环境因子,直接影响藻体生物量积累与目标产物合成效率。本研究进一步优化了光照与碳源培养策略,通过筛选适宜的光照强度、光照周期及碳源类型(葡萄糖、碳酸氢钠等),平衡了藻体光合作用与异源代谢之间的资源分配,既保证了莱茵衣藻的快速生长、提升了藻体生物量,又为(+)-诺卡酮的合成提供了充足的能量与碳骨架,有效促进了目标产物的胞内积累,解决了异源合成过程中“生长与合成失衡”的关键问题。
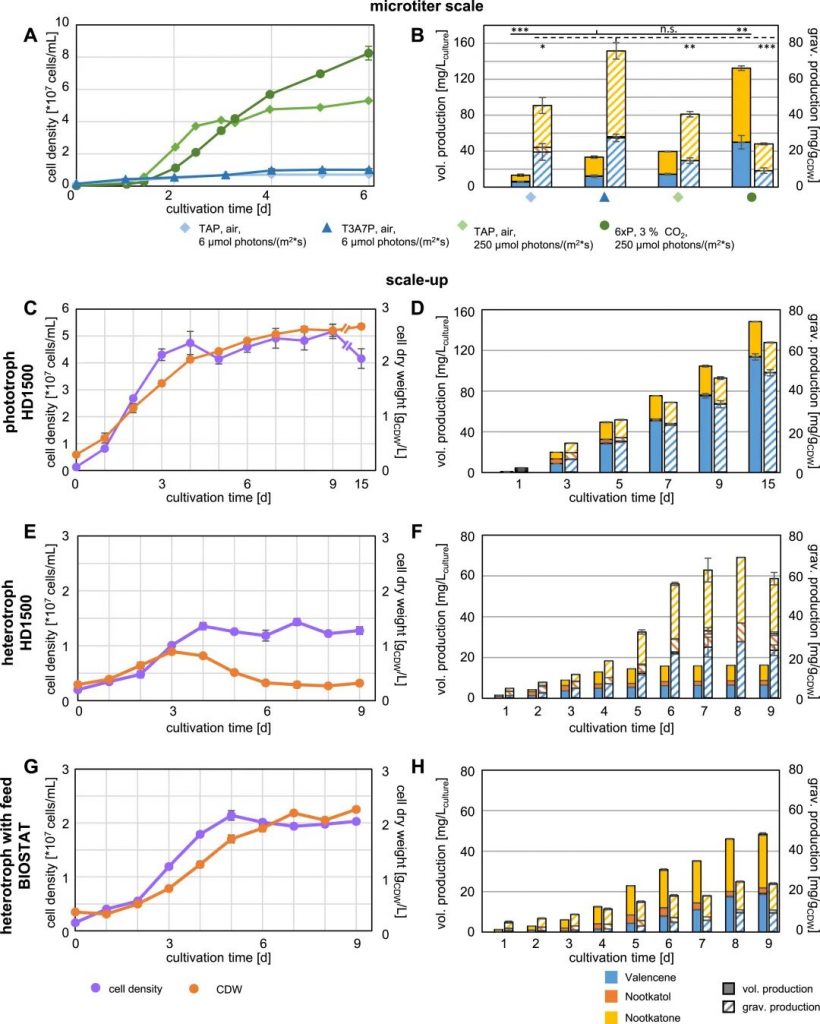
最终,本研究整合关键酶功能表征、MEP途径融合酶优化、叶绿体资源利用及光碳条件调控等多项代谢工程技术,在莱茵衣藻体系中实现了(+)-诺卡酮的高效异源合成,达到148 mg/L的体积产量与76 mg/gCDW(细胞干重)的重量产量,显著优于现有微藻异源合成倍半萜类化合物的产量水平。该研究不仅建立了高效、绿色的(+)-诺卡酮合成技术体系,更为基于微藻的绿色细胞工厂构建提供了新的思路与技术支撑,为高附加值萜类化合物的工业化生产开辟了可靠的技术路径,具有重要的理论研究价值与工业应用前景。
原文链接:Harnessing the MEP pathway for heterologous (+)-nootkatone biosynthesis in a green microalga under fine-tuned light and carbon regimes