萜类化合物是自然界中规模最大、结构最具多样性的天然产物家族,凭借其独特的生物活性,在医药、食品、化妆品及生物能源等多个领域展现出广泛的应用前景,是极具开发价值的高附加值天然产物。然而,传统依赖植物提取的生产方式存在显著局限,不仅萜类产物产量低下,且受植物生长周期长、自然资源储量有限、提取工艺复杂等因素制约,难以满足工业化大规模生产的需求,因此开发高效、可持续的替代生产方案成为行业迫切需求。
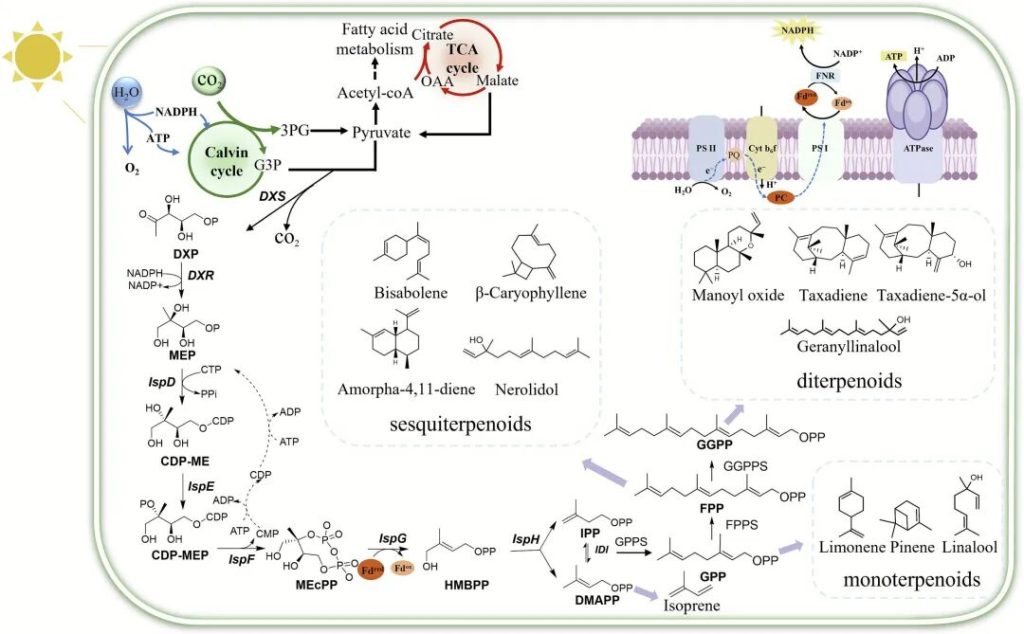
合成生物学技术的快速发展,为萜类化合物的绿色高效合成提供了新路径,其中开发高效微生物细胞工厂成为当前研究的热点。蓝藻作为一类光合自养原核生物,凭借其独特的生理代谢优势,成为萜类化合物合成的理想底盘微生物。与其他微生物相比,蓝藻自身具备天然的MEP(甲基赤藓糖醇磷酸)途径,可高效合成萜类化合物的关键前体物质,无需额外添加复杂碳源;其细胞内丰富的类囊体膜结构,能为异源表达的CYP450酶提供稳定的锚定位点,保障酶的活性;同时,蓝藻的光合电子传递链可持续供应萜类合成所需的充足NADPH,有效解决了异源合成过程中辅酶供应不足的难题,进一步提升萜类合成效率。
本文综述了近年来蓝藻萜类化合物生物合成领域的最新研究进展,系统分析了限制蓝藻高效合成萜类的关键瓶颈,主要包括萜类前体合成效率不足、异源酶活性偏低、产物积累过程中存在反馈抑制、细胞内代谢流分配不合理等。针对这些瓶颈,本文重点讨论了前沿合成生物学策略在蓝藻细胞工厂改造中的应用,包括CRISPR介导的精准基因编辑技术、RNA干扰调控技术、合成微生物共培养体系、酶分子改造工程及系统代谢工程等。
这些策略通过精准调控蓝藻体内的代谢网络,优化萜类合成途径,提升关键酶活性,解除产物反馈抑制,实现代谢流向萜类合成途径的高效分配,从而显著提升萜类化合物的产量。本文的综述旨在为开发高性能蓝藻细胞工厂提供理论支撑和技术参考,推动植物源生物活性萜类化合物及其他高附加值天然产物的可持续生物合成,助力相关产业的绿色转型升级。
原文链接:Engineering phototrophic cyanobacteria as a robust platform for production of plant-derived bioactive terpenoids




