炎症性肠病(Inflammatory Bowel Disease, IBD)是一类以肠道持续性炎症为核心特征的慢性胃肠道疾病,主要包括克罗恩病和溃疡性结肠炎,其发病机制复杂,与遗传、环境、免疫紊乱及肠道微生态失衡密切相关。临床研究表明,IBD患者常伴随肠道屏障功能受损,肠道黏膜完整性被破坏,同时出现肠道菌群失调,有害菌过度增殖、有益菌数量减少,进一步加剧肠道炎症反应,严重影响患者生活质量,且传统治疗方案难以实现长期有效控制。
目前,IBD的传统疗法主要依赖抗炎药物、免疫抑制剂等,但这类治疗方式普遍面临诸多瓶颈:一方面,肠道炎症微环境中存在大量活性氧(ROS),过度积累的ROS会加重肠道黏膜损伤,加剧氧化应激反应,降低治疗效果;另一方面,口服益生菌在穿越胃酸、胆汁等消化道屏障时易失活,且在炎症肠道内定植能力不足,难以充分发挥调控肠道菌群的作用,导致治疗效果有限,因此开发新型高效的IBD治疗策略迫在眉睫。
针对上述治疗困境,本研究创新性地构建了一种口服微纳米机器人SP@LP@AuCe,以螺旋藻(Spirulina platensis)作为天然微载体,搭载经AuCe双金属纳米酶修饰的植物乳杆菌(Lactobacillus plantarum),实现微藻、益生菌与纳米酶的协同作用,构建多模态治疗体系。该生物杂化机器人的设计充分发挥各组分的优势:螺旋藻作为天然载体,不仅具有良好的生物相容性和生物可降解性,还能通过光合作用产生氧气,为益生菌的存活和定植提供适宜微环境,同时其螺旋结构可提供推进动力,助力机器人在肠道内精准靶向炎症部位;AuCe双金属纳米酶具有高效的ROS清除能力,可特异性清除肠道炎症部位的过量活性氧,缓解氧化应激损伤,为肠道黏膜修复创造有利条件;植物乳杆菌作为有益益生菌,能够调节肠道菌群结构,促进有益菌增殖、抑制有害菌生长,恢复肠道微生态平衡,同时增强肠道屏障功能。
动物实验验证显示,在葡聚糖硫酸钠(DSS)诱导的IBD小鼠模型中,SP@LP@AuCe微纳米机器人展现出优异的治疗效果:能够显著减轻小鼠肠道炎症反应,降低炎症因子水平,有效修复受损的肠道黏膜屏障,恢复肠道组织完整性,同时显著调节肠道菌群组成,改善菌群失调状态,提升小鼠的存活率和健康水平。
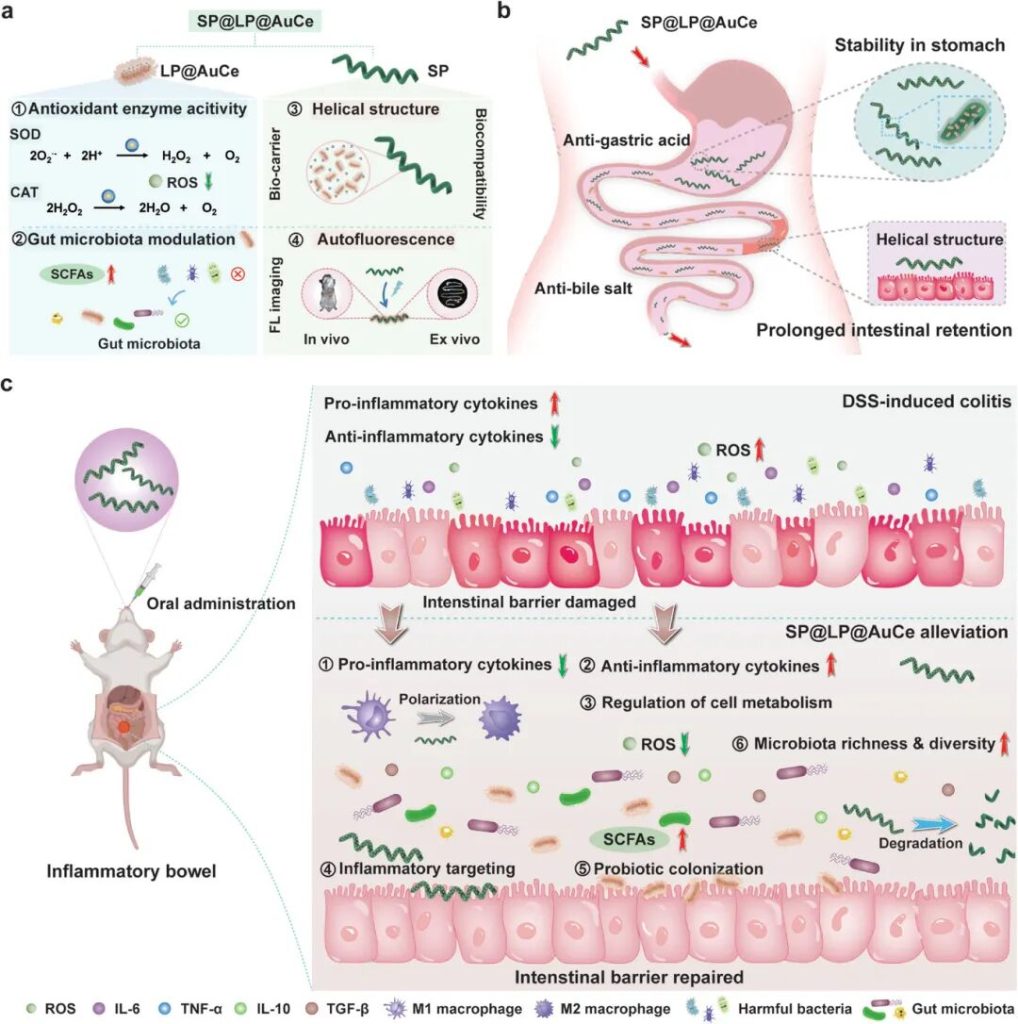
该研究的核心创新点在于将微藻、益生菌和纳米酶三者集成于微纳米机器人框架中,突破了传统疗法的局限,实现了“产氧供能-抗氧化损伤-菌群调控”的协同治疗,不仅提高了益生菌的肠道定植率和纳米酶的作用效率,还提升了治疗的靶向性和有效性。该策略为肠道炎症性疾病的治疗提供了一种全新的思路和有前景的新途径,有望推动肠道疾病治疗技术的革新,为临床IBD的高效治疗提供新的方案和理论支撑。
原文链接:A Microalgae-Probiotic-Nanozyme Robot for Alleviating Intestinal Inflammation and Microbiota Dysbiosis




