蓝藻(cyanobacteria)作为一类能够进行产氧光合作用的原核生物,凭借其光合效率高、代谢途径可调控、培养成本低等独特优势,在绿色生物制造、环境治理、能源开发及基础生物学研究等多个领域展现出巨大的应用潜力,是近年来合成生物学与微生物工程领域的研究热点之一。然而,尽管蓝藻相关研究已取得多项开创性进展,极大地推动了人们对光合机制、原核生物代谢调控的理解,但先进基因组编辑工具的匮乏,尤其是基于CRISPR系统的精准编辑技术,在蓝藻中的应用仍相对受限,这一现状严重制约了蓝藻遗传改造的效率与深度,成为阻碍蓝藻生物技术产业化发展的关键瓶颈。
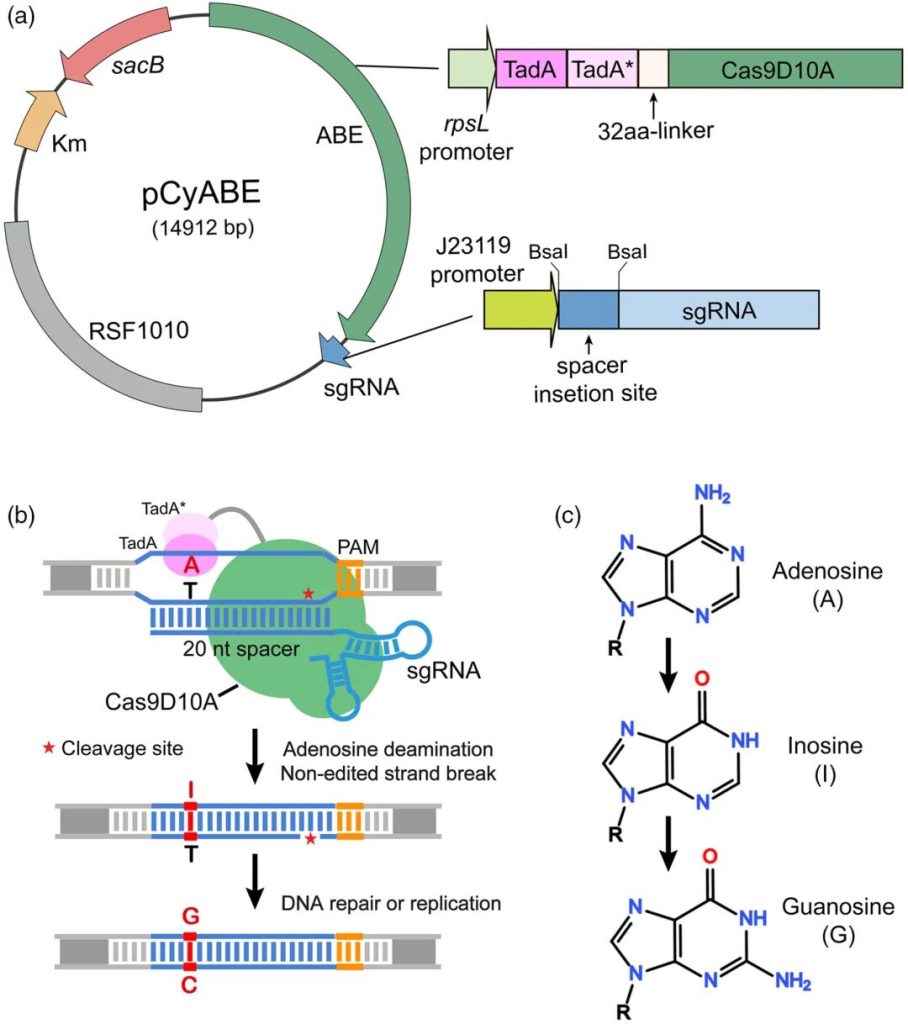
为解决这一技术难题,本研究针对性开发了pCyABE——一种专门用于蓝藻的全新腺嘌呤碱基编辑器,该工具可实现高效、精准的A·T碱基对向G·C碱基对的定向转换,填补了蓝藻高效腺嘌呤碱基编辑领域的空白。与传统基因组编辑技术不同,pCyABE系统创新性采用腺苷脱氨酶(TadA)与Cas9切口酶(nickase)的融合蛋白作为核心功能组件,其最大优势在于无需引入DNA双链断裂(DSB),也无需提供外源供体模板,即可完成精准的碱基替换,有效规避了双链断裂可能引发的基因组不稳定、随机插入缺失(indel)等副作用,显著提升了编辑的精准度与安全性。
为验证pCyABE系统的编辑效能与通用性,研究人员在两种模式蓝藻菌株——集胞藻Synechocystis sp. PCC 6803与念珠藻Anabaena sp. PCC 7120中开展了系统的验证实验。实验结果表明,该编辑器在两种不同生理特性的蓝藻中均表现出较高的编辑效率,编辑成功率稳定且可控,充分证明了pCyABE工具具有广泛的物种适用性,可满足不同蓝藻菌株的遗传编辑需求。
进一步的功能探究显示,pCyABE系统具备显著的技术优势:其一,支持多位点同时编辑,可实现多个靶基因的同步精准改造,大幅提升遗传操作的效率;其二,可通过特异性破坏基因起始密码子的方式,快速实现靶基因的沉默,为蓝藻基因功能研究提供了高效、便捷的技术手段;其三,该系统具有较低的脱靶活性,通过严格的序列特异性识别,最大限度降低了非靶标位点的意外编辑,保障了编辑的特异性;此外,pCyABE还可通过蔗糖反选策略实现编辑器元件的高效去除,避免了编辑工具持续存在对蓝藻细胞代谢的干扰,为后续的遗传改造与表型分析提供了便利。
综上,本研究开发的pCyABE腺嘌呤碱基编辑器,为蓝藻的基础研究与生物技术应用提供了一个灵活、高效、精准的基因组编辑平台,不仅显著扩展了蓝藻的遗传操作工具箱,也为蓝藻的定向遗传改造、代谢途径优化及合成生物学研究提供了重要的技术支撑,有望推动蓝藻在绿色生物制造、新能源开发等领域的产业化应用进程。
原文链接:Programmable adenine base editing in cyanobacteria using an engineered TadA-Cas9 fusion




